近年來,細(xì)胞和基因治療顯示出巨大的輝煌,在不久的將來,批準(zhǔn)的細(xì)胞和基因療法產(chǎn)品數(shù)量將急劇增加。2019 年初,美國食品藥品監(jiān)督管理局宣布了未來細(xì)胞治療的發(fā)展計(jì)劃。預(yù)計(jì)到 2025 年,該領(lǐng)域每年將有 10-20 種新藥獲批,包括細(xì)胞和基因治療產(chǎn)品。近日,據(jù)外媒報(bào)道,預(yù)計(jì)到 2023 年底,美國、歐洲或兩者將批準(zhǔn) 13 種新的細(xì)胞或基因療法。

隨著 CRISPR 等基因組編輯技術(shù)的出現(xiàn)和人們對免疫學(xué)認(rèn)識的加深,以及特殊生物樣品和材料的培養(yǎng)、制造、運(yùn)輸、儲存和加工的優(yōu)化,細(xì)胞治療領(lǐng)域正在發(fā)生革命性的變化。
目前,CAR-T 等免疫細(xì)胞療法為一些腫瘤的治療帶來了新的選擇。然而,細(xì)胞技術(shù)的發(fā)展和不同干細(xì)胞的應(yīng)用,如脂肪干細(xì)胞、間充質(zhì)干細(xì)胞和誘導(dǎo)多能干細(xì)胞,將為神經(jīng)系統(tǒng)、肌肉骨骼和皮膚病等腫瘤以外的疾病提供更好的選擇。
細(xì)胞療法的獨(dú)特應(yīng)用和治療優(yōu)勢
細(xì)胞療法是一種以細(xì)胞為基礎(chǔ),以活細(xì)胞為活性藥物治療疾病的治療方法。細(xì)胞療法是目前臨床上最有前途的治療方法,有可能治愈多種難治性疾病。與其他療法相比,細(xì)胞療法具有獨(dú)特的臨床應(yīng)用和治療優(yōu)勢。
首先,活細(xì)胞可以動態(tài)消除惡性腫瘤,再生組織細(xì)胞,恢復(fù)受損的組織功能,并根據(jù)自身情況增加身體抵抗疾病的能力。
其次,活細(xì)胞可以對系統(tǒng)和局部的化學(xué)、物理和生物變化做出反應(yīng)。
此外,活細(xì)胞更容易突破生物屏障,實(shí)現(xiàn)精確的分子靶向功能,準(zhǔn)確定位細(xì)胞和組織,并與其相互作用以實(shí)現(xiàn)治療功能。
全球細(xì)胞療法的發(fā)展概況
目前,全球細(xì)胞治療市場主要由干細(xì)胞、組織特異性細(xì)胞和血細(xì)胞組成。
干細(xì)胞療法
目前,批準(zhǔn)用于臨床的干細(xì)胞療法包括造血干細(xì)胞(HSCs)、間充質(zhì)干細(xì)胞(MSC)和角膜緣干細(xì)胞(LSCs)。造血干細(xì)胞(HSC)產(chǎn)品主要被批準(zhǔn)用于治療血液疾病。間充質(zhì)干細(xì)胞(MSCs)治療適用于多種疾病,包括心血管疾病、移植物抗宿主病(GvHD)、退行性疾病、炎癥性腸病和其他難治性疾病。角膜緣干細(xì)胞(LSC)產(chǎn)品僅被批準(zhǔn)用于角膜緣干細(xì)胞缺陷。

▲ 全球獲批上市的近 20 款干細(xì)胞產(chǎn)品
組織特異性細(xì)胞療法
組織特異性細(xì)胞主要用于再生醫(yī)學(xué)和組織工程,如用于治療熱燒傷的自體皮膚細(xì)胞(即角質(zhì)形成細(xì)胞、成纖維細(xì)胞和黑素細(xì)胞),用于治療糖尿病下肢靜脈潰瘍和足潰瘍的雙層活細(xì)胞皮膚替代物,以及用于修復(fù)軟骨缺損的自體軟骨細(xì)胞支架。
血細(xì)胞療法
包括白細(xì)胞、紅細(xì)胞和血小板。然而,目前只有 T 細(xì)胞和 DC 細(xì)胞被批準(zhǔn)用于臨床治療。大多數(shù) T 細(xì)胞產(chǎn)物是嵌合抗原受體(CAR-T)治療惡性血液病,而 DC 細(xì)胞治療被用作癌癥疫苗。
根據(jù)近年來全球細(xì)胞治療臨床研究綜述,五年前針對間充質(zhì)干細(xì)胞的臨床試驗(yàn)和研究數(shù)量排名第一。近年來,對單個 T 細(xì)胞進(jìn)行測試的研究數(shù)量遠(yuǎn)遠(yuǎn)超過了對所有干細(xì)胞和組織特異性細(xì)胞的研究數(shù)量。這一重大轉(zhuǎn)變主要是由于 CAR-T 療法的成功臨床應(yīng)用(見下圖)。從統(tǒng)計(jì)數(shù)據(jù)來看,T 細(xì)胞主導(dǎo)了當(dāng)前細(xì)胞治療的臨床研究,其次是干細(xì)胞、樹突狀細(xì)胞、自然殺傷細(xì)胞、微生物、紅細(xì)胞、單核細(xì)胞和血小板。
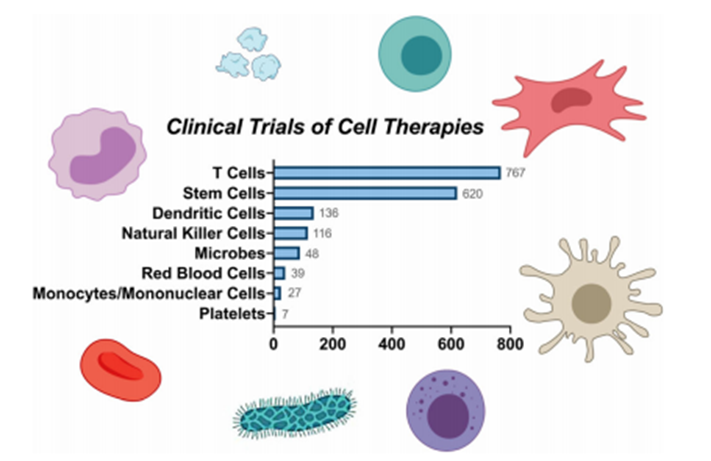
▲ 臨床試驗(yàn)中的各種類型的細(xì)胞療法
全球 T 免疫細(xì)胞治療的發(fā)展概況
截至目前,全球市場上共有 7 種 CAR-T 免疫細(xì)胞治療產(chǎn)品。
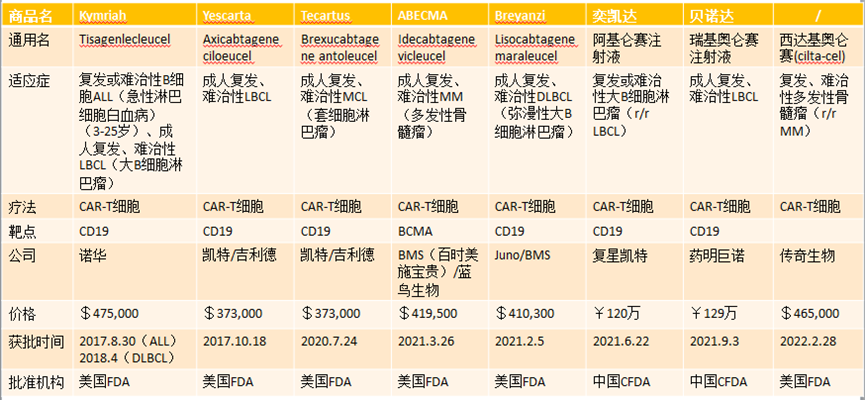 此外,其他 T 細(xì)胞療法已被用于治療實(shí)體瘤。
此外,其他 T 細(xì)胞療法已被用于治療實(shí)體瘤。
ImmunCell-LC 于 2007 年獲得 KFDA 批準(zhǔn),是一種基于自體細(xì)胞因子誘導(dǎo)殺傷(CIK)細(xì)胞的免疫療法。主要用于腫瘤切除后的輔助治療。它可以通過去除殘留的腫瘤細(xì)胞來治療肝細(xì)胞癌、腦腫瘤和胰腺癌癥。
目前,T 淋巴細(xì)胞治療的臨床試驗(yàn)如下圖所示。T 淋巴細(xì)胞是所有細(xì)胞治療試驗(yàn)中研究最多的細(xì)胞類型,占所有試驗(yàn)的 45%。根據(jù)它們的狀態(tài),它們被分為轉(zhuǎn)基因(GM)和非轉(zhuǎn)基因(NGM)。轉(zhuǎn)基因(GM)細(xì)胞根據(jù)其受體類型分為嵌合抗原受體(CAR)和 T 細(xì)胞受體(TCR),而非轉(zhuǎn)基因(NGM)細(xì)胞則根據(jù)其靶標(biāo)類型分為靶向腫瘤相關(guān)抗原(TAA)和病毒抗原(VST)。如果沒有明確的受體或靶標(biāo),則將其歸類為“其他”。
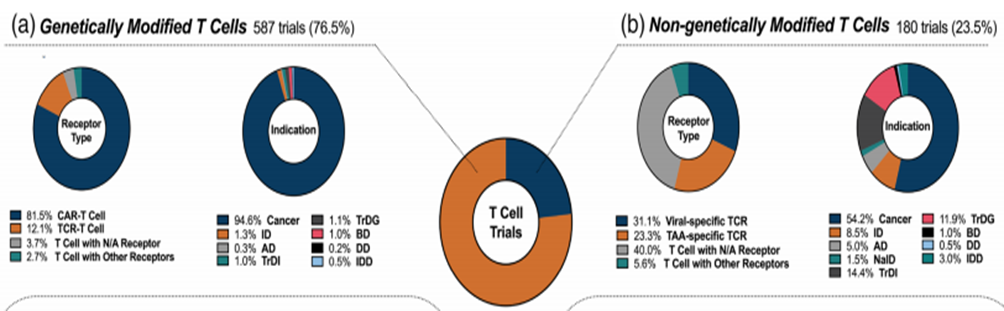
▲ T 細(xì)胞臨床試驗(yàn)的現(xiàn)狀
如圖所示,在目前針對 T 細(xì)胞的臨床試驗(yàn)中,轉(zhuǎn)基因(GM)T 細(xì)胞占 76.5%,而非轉(zhuǎn)基因(NGM)T 細(xì)胞約占 23.5%。轉(zhuǎn)基因類別試驗(yàn)根據(jù)轉(zhuǎn)基因受體的類型進(jìn)一步分類。其中,靶向 CAR-T 細(xì)胞治療的臨床試驗(yàn)占轉(zhuǎn)基因(GM)T 細(xì)胞的 81.5%,TCR-T 細(xì)胞的 12.1%,具有不適當(dāng)受體(N/A)的 T 細(xì)胞的 3.7%,其他 T 細(xì)胞受體的 2.7%,TAA 特異性 T 淋巴細(xì)胞的 23.3%,具有不當(dāng)受體(N/A)的 T 細(xì)胞的 40.0%,以及其他 T 細(xì)胞靶點(diǎn)的 5.6%。
CAR-T 細(xì)胞治療
目前,絕大多數(shù)已批準(zhǔn)的 CAR-T 療法都專注于 CD19 靶點(diǎn)。此外,BCMA、CD22 和 CD20 也已成為流行的靶點(diǎn)。
由于缺乏明確的細(xì)胞外抗原靶點(diǎn)、T 細(xì)胞浸潤不足以及難以克服免疫抑制的腫瘤微環(huán)境,CAR-T 治療在實(shí)體瘤中仍然是一個巨大的挑戰(zhàn)。目前,約 24% 的臨床試驗(yàn)靶點(diǎn)仍用于實(shí)體瘤。最常見的靶點(diǎn)是 GD2(神經(jīng)母細(xì)胞瘤和黑色素瘤)、HER2(轉(zhuǎn)移性乳腺癌)和 GPC3(癌癥)。
除了研究不同的腫瘤細(xì)胞外抗原靶點(diǎn)外,CAR-T 細(xì)胞治療的不同給藥方法也是研究熱點(diǎn)。目前,CAR-T 治療的主要給藥途徑仍然是靜脈給藥,而其他給藥途徑也在研究中,如腹膜內(nèi)、腫瘤內(nèi)、肝內(nèi)動脈、胰腺內(nèi)和胸膜內(nèi)給藥。不同的給藥方法可能在預(yù)防 T 細(xì)胞衰竭、提高靶點(diǎn)特異性和促進(jìn)組織浸潤方面具有優(yōu)勢,這可能會增加 CAR-T 目前在實(shí)體瘤治療中的應(yīng)用。
TCR-T 細(xì)胞治療
TCR-T 細(xì)胞療法通過與 MHC 的有效相互作用激活宿主的免疫系統(tǒng)。與 CAR-T 細(xì)胞療法只能識別腫瘤表面的特異性抗原不同,TCR-T 細(xì)胞療法可以識別細(xì)胞內(nèi)的腫瘤特異性抗原,使 TCR-T 細(xì)胞療法在腫瘤治療中更有效。NY-ESO-1 是最常見的靶抗原,在許多癌癥中表達(dá),包括骨髓瘤、黑色素瘤等。其他腫瘤相關(guān)抗原,如 PRAME 和 MAGE 蛋白,黑色素瘤分化抗原 MART-1 和 gp100,以及最近的癌癥驅(qū)動因素,如 WT1、KRAS 和 TP53,也是流行的 TCR-T 靶點(diǎn)。
病毒特異性 T 細(xì)胞(VST-T)治療
VST 目前正在進(jìn)行治療癌癥、移植相關(guān)疾病和感染的臨床研究。VST 可以通過識別 MHC 上的病毒表位來消除病毒誘導(dǎo)的癌癥,還可以用于治療與癌癥和/或移植無關(guān)的病毒感染,如艾滋病病毒和嚴(yán)重急性呼吸綜合征冠狀病毒(SARS 冠狀病毒 2 型)。
TAA 特異性 T 淋巴細(xì)胞治療
目前,大約 2/3 的 TAA 特異性 T 淋巴細(xì)胞療法被設(shè)計(jì)用于治療實(shí)體瘤,一些試驗(yàn)?zāi)壳疤幱谂R床試驗(yàn)的第二階段。
總之,T 淋巴細(xì)胞治療癌癥的臨床試驗(yàn)?zāi)壳罢谂畈l(fā)展。T 淋巴細(xì)胞療法不同于傳統(tǒng)的治療疾病的方法,是一種有效的治療方法,已被 FDA、EMA 和世界各地的其他監(jiān)管機(jī)構(gòu)批準(zhǔn)用于治療癌癥。
然而,仍然存在重大挑戰(zhàn),包括生物來源的安全性和免疫原性、生物功能的異質(zhì)性、細(xì)胞治療后生物活性的維持、最佳遞送方法的選擇,以及細(xì)胞治療劑的制造和調(diào)節(jié)方面的挑戰(zhàn)。
隨著臨床研究的進(jìn)展,基于 T 免疫細(xì)胞的治療有望成為治療更多疾病的新選擇。
全球細(xì)胞治療監(jiān)管政策促進(jìn)發(fā)展
從第一次干細(xì)胞移植到今天的工程細(xì)胞療法獲得批準(zhǔn),花了將近 50 年的時(shí)間。隨著研究和調(diào)控的逐漸發(fā)展和成熟,人們可以看到下一代基于細(xì)胞的治療可以在更短的時(shí)間內(nèi)惠及更多患者。目前,世界各地正在采取不同的措施來加快創(chuàng)新新藥的審批。
例如,美國食品藥品監(jiān)督管理局有幾種加快審批的方法,如再生醫(yī)學(xué)高級治療資格認(rèn)證(RMAT)、快速通道資格認(rèn)證等。美國食品藥品監(jiān)管局表示,未來將加強(qiáng)與產(chǎn)品開發(fā)商的溝通與合作,以最大限度地利用這些渠道。
在中國,自 2018 年 11 月以來,中國新藥臨床試驗(yàn)正式從以前的審批制度轉(zhuǎn)向默示許可,從“點(diǎn)頭制”審批轉(zhuǎn)向“搖頭制”審批時(shí)代,這意味著中國新藥臨床實(shí)驗(yàn)行政許可將進(jìn)入更高效的審查模式。
在過去幾年中,美國、澳大利亞、歐盟、日本、韓國、中國和其他地區(qū)已經(jīng)批準(zhǔn)推出新的細(xì)胞治療產(chǎn)品,包括免疫細(xì)胞治療產(chǎn)品和干細(xì)胞治療產(chǎn)品。未來,隨著監(jiān)管、審批和支付方式的逐步完善,這類產(chǎn)品的發(fā)布速度將更快,市場滲透率將更大。這意味著更多的患者將能夠使用細(xì)胞治療產(chǎn)品。
免責(zé)聲明:
我們尊重原創(chuàng),也注重分享。圖文來源網(wǎng)絡(luò),版權(quán)歸原作者所有,如涉及作品內(nèi)容、版權(quán)或其它問題,請聯(lián)系我們刪除!


 閩公網(wǎng)安備 35020602002648 號
閩公網(wǎng)安備 35020602002648 號 QQ 客服
QQ 客服
